Världen vi lever i är ofattbart vacker och full av många olika processer som sätter livets kurs. Alla dessa processer studeras av den välbekanta vetenskapen - fysik. Det ger en möjlighet att få åtminstone en uppfattning om universums ursprung. I den här artikeln kommer vi att överväga ett sådant koncept som molekylär kinetisk teori, dess ekvationer, typer och formler. Men innan du går vidare till en djupare studie av dessa frågor måste du klargöra själva innebörden av fysiken och de områden den studerar.
Vad är fysik?

Det här är faktiskt en mycket omfattande vetenskap och kanske en av de mest grundläggande i mänsklighetens historia. Till exempel, om samma datavetenskap är förknippad med nästan alla områden av mänsklig aktivitet, oavsett om det är beräkningsdesign eller skapandet av tecknade serier, så är fysiken livet självt, en beskrivning av dess komplexa processer och flöden. Låt oss försöka reda ut dess innebörd och förenkla förståelsen så mycket som möjligt.
SåSåledes är fysiken en vetenskap som sysslar med studiet av energi och materia, sambanden mellan dem, förklaringen av många processer som sker i vårt enorma universum. Den molekylär-kinetiska teorin om materiens struktur är bara en liten droppe i havet av teorier och grenar av fysiken.
Energi, som denna vetenskap studerar i detalj, kan representeras i en mängd olika former. Till exempel i form av ljus, rörelse, gravitation, strålning, elektricitet och många andra former. Vi kommer i denna artikel att beröra den molekylära kinetiska teorin om dessa formers struktur.
Studiet av materia ger oss en uppfattning om materiens atomstruktur. Det följer förresten av den molekylär-kinetiska teorin. Vetenskapen om materiens struktur låter oss förstå och hitta meningen med vår existens, orsakerna till livets uppkomst och själva universum. Låt oss fortfarande försöka studera den molekylära kinetiska teorin om materia.
För det första behövs en introduktion för att helt förstå terminologin och eventuella slutsatser.
fysikämnen
När man svarar på frågan om vad molekylär-kinetisk teori är, kan man inte annat än prata om delar av fysiken. Var och en av dessa behandlar den detaljerade studien och förklaringen av ett visst område av mänskligt liv. De klassificeras enligt följande:
- Mekanik, som är uppdelad i ytterligare två sektioner: kinematik och dynamik.
- Statisk.
- Termodynamik.
- Molekylär sektion.
- Elektrodynamik.
- Optik.
- Kvanternas fysik och atomkärnan.
Låt oss prata specifikt om molekylärfysik, eftersom den är baserad på den molekylär-kinetiska teorin.
Vad är termodynamik?
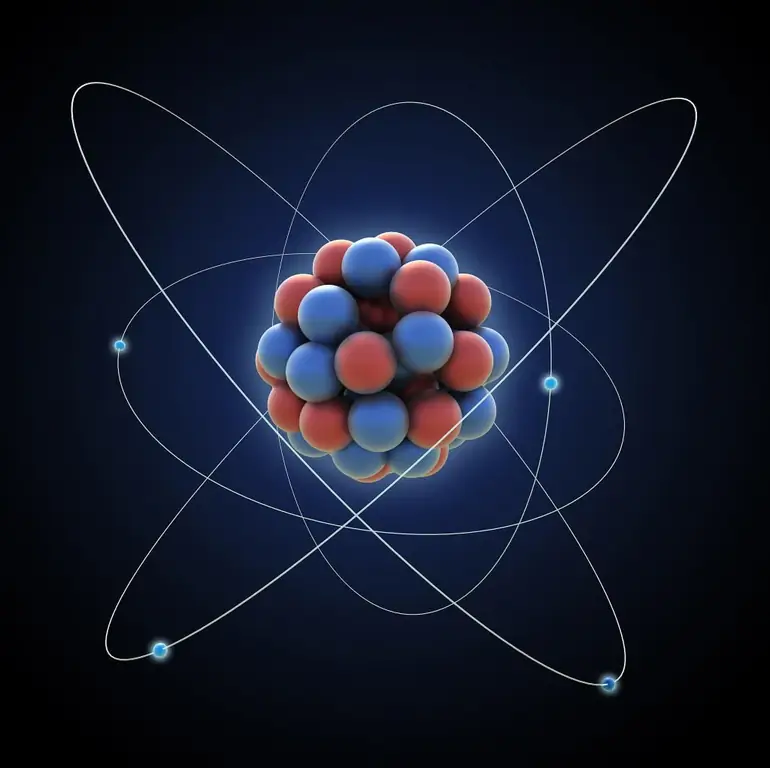
I allmänhet är den molekylära delen och termodynamiken närbesläktade grenar av fysiken, som uteslutande studerar den makroskopiska komponenten av det totala antalet fysiska system. Det är värt att komma ihåg att dessa vetenskaper beskriver exakt det inre tillståndet hos kroppar och ämnen. Till exempel deras tillstånd under uppvärmning, kristallisation, förångning och kondensation, på atomnivå. Molekylär fysik är med andra ord vetenskapen om system som består av ett stort antal partiklar: atomer och molekyler.
Det var dessa vetenskaper som studerade huvudbestämmelserna i den molekylära kinetiska teorin.
Även under sjunde årskursen bekantade vi oss med begreppen mikro- och makrovärldar, system. Det kommer inte att vara överflödigt att uppdatera dessa termer i minnet.
Mikrovärlden, som vi kan se av själva namnet, består av elementarpartiklar. Detta är med andra ord de små partiklarnas värld. Deras storlekar mäts i intervallet från 10-18 m till 10-4 m, och tiden för deras faktiska tillstånd kan nå både oändligt och oproportionerligt små intervall, till exempel 10-20 s.
Macroworld betraktar kroppar och system av stabila former, bestående av många elementarpartiklar. Sådana system står i proportion till vår mänskliga storlek.
Dessutom finns det en sådan sak som en megavärld. Den består av enorma planeter, kosmiska galaxer och komplex.
Grundläggandeteori
Nu när vi har sammanfattat lite och kommit ihåg fysikens grundläggande termer, kan vi gå direkt till huvudämnet för den här artikeln.
Molekylär-kinetisk teori dök upp och formulerades för första gången på artonhundratalet. Dess essens ligger i det faktum att den i detalj beskriver strukturen av något ämne (oftare strukturen hos gaser än fasta och flytande kroppar), baserat på tre grundläggande bestämmelser som samlades in från antaganden från sådana framstående vetenskapsmän som Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov och många andra.
De huvudsakliga bestämmelserna i den molekylära kinetiska teorin låter så här:
- Absolut alla ämnen (oavsett om de är flytande, fasta eller gasformiga) har en komplex struktur, bestående av mindre partiklar: molekyler och atomer. Atomer kallas ibland "elementära molekyler".
- Alla dessa elementarpartiklar är alltid i ett tillstånd av kontinuerlig och kaotisk rörelse. Var och en av oss har stött på ett direkt bevis på detta förslag, men har troligen inte fäst stor vikt vid det. Till exempel såg vi alla mot bakgrund av solens strålar att dammpartiklar hela tiden rör sig i en kaotisk riktning. Detta beror på det faktum att atomerna producerar ömsesidiga tryck med varandra, vilket ständigt förmedlar kinetisk energi till varandra. Detta fenomen studerades första gången 1827, och det fick sitt namn efter upptäckaren - "Brownian motion".
- Alla elementarpartiklar är i färd med att kontinuerligt interagera med varandra medvissa krafter som har en elektrisk sten.
Det är värt att notera att ett annat exempel som beskriver position nummer två, vilket också kan gälla till exempel för den molekylära kinetiska teorin om gaser, är diffusion. Vi stöter på det i vardagen och i flera tester och kontroller, så det är viktigt att ha en uppfattning om det.
Tänk först på följande exempel:
Läkaren spillde av misstag alkohol från en kolv på bordet. Eller så kanske du tappade din parfymflaska och den spred sig över hela golvet.
Varför, i dessa två fall, kommer både lukten av alkohol och lukten av parfym att fylla hela rummet efter en tid, och inte bara området där innehållet av dessa ämnen spilldes ut?
Svaret är enkelt: diffusion.
Diffusion - vad är det? Hur flyter det?

Detta är en process där partiklarna som utgör en viss substans (vanligtvis en gas) tränger in i de intermolekylära tomrummen i en annan. I våra exempel ovan hände följande: på grund av termisk, det vill säga kontinuerlig och dissocierad rörelse, föll alkohol- och/eller parfymmolekyler in i luckorna mellan luftmolekylerna. Gradvis, under påverkan av kollision med atomer och luftmolekyler, sprider de sig runt i rummet. Förresten, diffusionsintensiteten, det vill säga hastigheten på dess flöde, beror på densiteten hos de ämnen som är involverade i diffusionen, såväl som på rörelseenergin hos deras atomer och molekyler, kallad kinetisk. Ju större kinetisk energi är, desto högre hastighet har dessa molekyler respektive intensitet.
Den snabbaste diffusionsprocessen kan kallas diffusion i gaser. Detta beror på det faktum att gasen inte är homogen i sin sammansättning, vilket innebär att intermolekylära hålrum i gaser upptar en betydande mängd utrymme, respektive, och processen att få in atomer och molekyler av ett främmande ämne i dem går lättare och snabbare.
Denna process är lite långsammare i vätskor. Upplösningen av sockerbitar i en mugg te är bara ett exempel på diffusion av ett fast ämne i en vätska.
Men den längsta tiden är diffusion i kroppar med en solid kristallin struktur. Detta är exakt så, eftersom strukturen hos fasta ämnen är homogen och har ett starkt kristallgitter, i vilka cellerna atomerna i det fasta ämnet vibrerar. Till exempel, om ytorna på två metallstänger rengörs väl och sedan bringas i kontakt med varandra, kommer vi efter tillräckligt lång tid att kunna upptäcka bitar av en metall i den andra, och vice versa.
Liksom alla andra grundläggande avsnitt är fysikens grundläggande teori uppdelad i separata delar: klassificering, typer, formler, ekvationer och så vidare. Således har vi lärt oss grunderna i molekylär kinetisk teori. Detta innebär att du säkert kan gå vidare till behandlingen av enskilda teoretiska block.
Molekylär-kinetisk teori om gaser
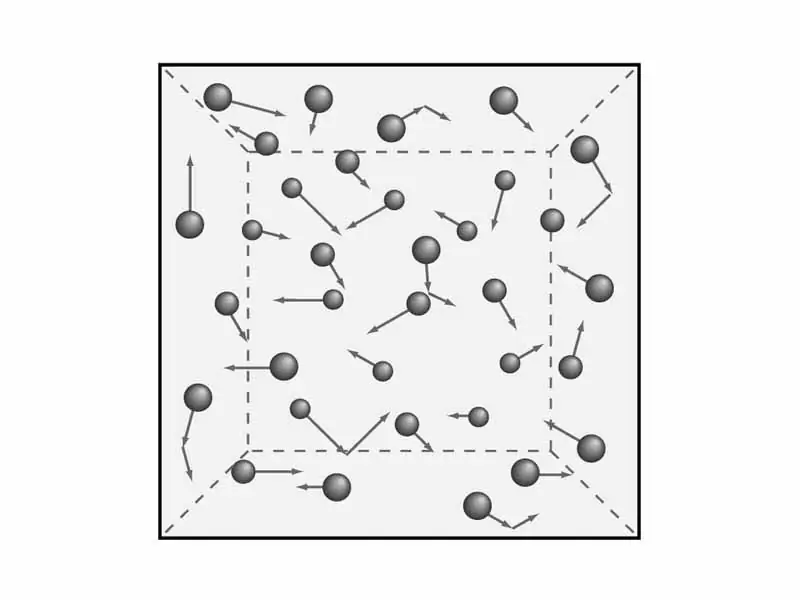
Det finns ett behov av att förstå bestämmelserna i gasteorin. Som vi sa tidigare kommer vi att överväga de makroskopiska egenskaperna hos gaser, såsom tryck och temperatur. Detta ärkommer att behövas senare för att härleda ekvationen för den molekylär-kinetiska teorin för gaser. Men matematik - senare, och nu, låt oss ta itu med teori och, följaktligen, fysik.
Forskare har formulerat fem bestämmelser i den molekylära teorin om gaser, som tjänar till att förstå den kinetiska modellen för gaser. De låter så här:
- Alla gaser är uppbyggda av elementarpartiklar som inte har en viss storlek, men har en viss massa. Med andra ord är volymen av dessa partiklar minimal jämfört med längden mellan dem.
- Atomer och molekyler av gaser har praktiskt taget ingen potentiell energi, respektive enligt lagen är all energi lika med kinetisk.
- Vi har redan bekantat oss med den här positionen tidigare - Brownsk rörelse. Det vill säga gaspartiklar är alltid i kontinuerlig och kaotisk rörelse.
- Absolut alla inbördes kollisioner av gaspartiklar, åtföljda av budskapet om hastighet och energi, är helt elastiska. Detta innebär att det inte sker någon energiförlust eller skarpa hopp i deras kinetiska energi under en kollision.
- Under normala förhållanden och konstant temperatur är medelenergin för partikelrörelser för nästan alla gaser densamma.
Vi kan skriva om den femte positionen genom denna typ av ekvation av den molekylär-kinetiska teorin om gaser:
E=1/2mv^2=3/2kT, där k är Boltzmann-konstanten; T - temperatur i Kelvin.
Denna ekvation får oss att förstå sambandet mellan hastigheten hos elementarpartiklar av gas och deras absoluta temperatur. Följaktligen, desto högre är deras absolutatemperatur, desto högre hastighet och kinetisk energi.
Gastryck
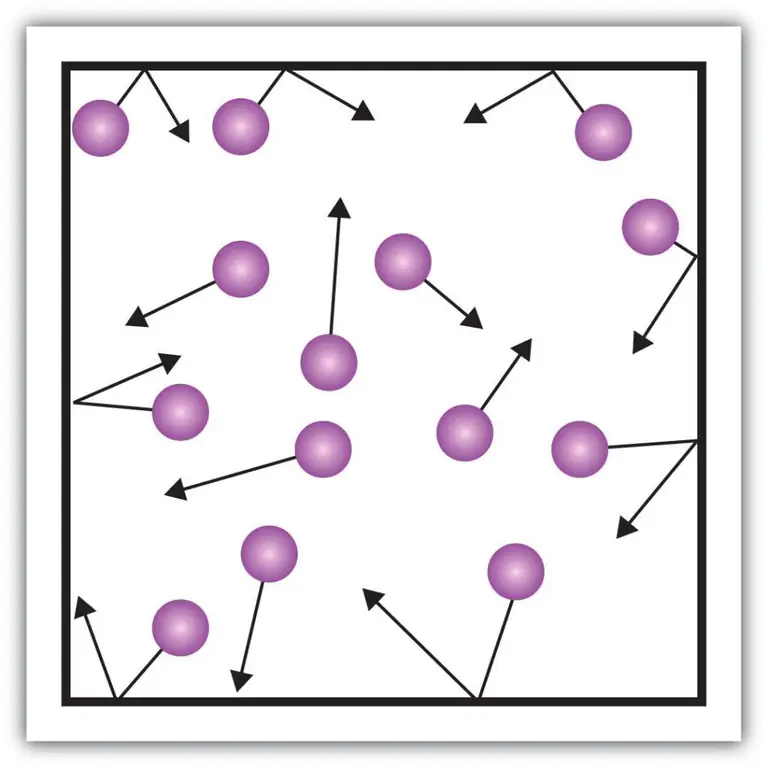
Sådana makroskopiska komponenter i egenskapen, såsom trycket hos gaser, kan också förklaras med hjälp av kinetisk teori. För att göra detta, låt oss föreställa oss följande exempel.
Låt oss anta att en molekyl av en gas finns i en låda, vars längd är L. Låt oss använda bestämmelserna i gasteorin som beskrivs ovan och ta hänsyn till det faktum att molekylsfären endast rör sig längs x -axel. Således kommer vi att kunna observera processen för elastisk kollision med en av kärlets (låda) väggar.
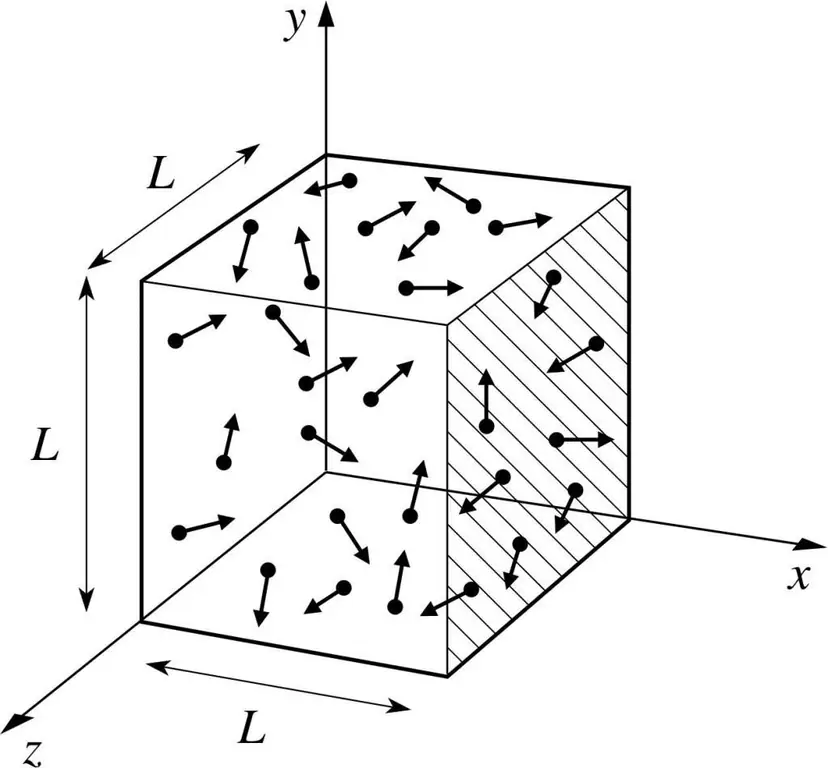
Dymn för den pågående kollisionen, som vi vet, bestäms av formeln: p=mv, men i det här fallet kommer denna formel att anta en projektionsform: p=mv(x).
Eftersom vi endast betraktar dimensionen på x-axeln, det vill säga x-axeln, kommer den totala förändringen i momentum att uttryckas med formeln: mv(x) - m(-v(x))=2mv(x).
Tänk sedan på kraften som utövas av vårt objekt med hjälp av Newtons andra lag: F=ma=P/t.
Från dessa formler uttrycker vi trycket från gassidan: P=F/a;
Låt oss nu ersätta kraftuttrycket i den resulterande formeln och få: P=mv(x)^2/L^3.
Därefter kan vår färdiga tryckformel skrivas för det N:te antalet gasmolekyler. Med andra ord kommer det att se ut så här:
P=Nmv(x)^2/V, där v är hastighet och V är volym.
Låt oss nu försöka lyfta fram några grundläggande bestämmelser om gastryck:
- Det visar sig genomkollisioner av molekyler med molekyler i väggarna på föremålet där det befinner sig.
- Tryckets storlek är direkt proportionell mot kraften och hastigheten för molekylers anslag mot kärlets väggar.
Några korta slutsatser om teori
Innan vi går vidare och överväger den grundläggande ekvationen för molekylär kinetisk teori, ger vi dig några korta slutsatser från ovanstående punkter och teori:
- Månget på den genomsnittliga rörelseenergin för dess atomer och molekyler är den absoluta temperaturen.
- När två olika gaser har samma temperatur, har deras molekyler samma genomsnittliga kinetiska energi.
- Gaspartiklars energi är direkt proportionell mot medelkvadrathastigheten: E=1/2mv^2.
- Även om gasmolekyler har en genomsnittlig kinetisk energi respektive en medelhastighet, rör sig enskilda partiklar med olika hastigheter: vissa snabba, vissa långsamma.
- Ju högre temperatur, desto högre hastighet har molekylerna.
- Hur många gånger vi ökar temperaturen på gasen (till exempel fördubblas), ökar rörelseenergin för dess partiklar lika många gånger (fördubblas).
Grundläggande ekvation och formler

Den grundläggande ekvationen för den molekylära kinetiska teorin låter dig fastställa förhållandet mellan mikrovärldens kvantiteter och följaktligen de makroskopiska, det vill säga uppmätta, kvantiteterna.
En av de enklaste modellerna som molekylär teori kan överväga är den ideala gasmodellen.
Det kan man sägadetta är en sorts imaginär modell studerad av den molekylära kinetiska teorin för en idealgas, där:
- de enklaste gaspartiklarna anses vara perfekt elastiska bollar som interagerar både med varandra och med molekylerna i väggarna i vilket kärl som helst i endast ett fall - en absolut elastisk kollision;
- attraktionskrafterna inuti gasen saknas, eller så kan de faktiskt försummas;
- element i gasens inre struktur kan tas som materiella punkter, det vill säga deras volym kan också försummas.
Med tanke på en sådan modell skrev den tyskfödde fysikern Rudolf Clausius en formel för gastryck genom förhållandet mellan mikro- och makroskopiska parametrar. Det ser ut som:
p=1/3m(0)nv^2.
Senare kommer denna formel att kallas som den grundläggande ekvationen för den molekylär-kinetiska teorin om en idealgas. Den kan presenteras i flera olika former. Vår plikt är nu att visa sektioner som molekylfysik, molekylär kinetisk teori och därmed deras kompletta ekvationer och typer. Därför är det vettigt att överväga andra varianter av grundformeln.
Vi vet att den genomsnittliga energin som kännetecknar gasmolekylernas rörelse kan hittas med formeln: E=m(0)v^2/2.
I det här fallet kan vi ersätta uttrycket m(0)v^2 i den ursprungliga tryckformeln med den genomsnittliga kinetiska energin. Som ett resultat av detta kommer vi att ha möjlighet att sammanställa grundekvationen för den molekylära kinetiska teorin för gaser i följande form: p=2/3nE.
Dessutom vet vi alla att uttrycket m(0)n kan skrivas som en produkt av två kvotienter:
m/NN/V=m/V=ρ.
Efter dessa manipulationer kan vi skriva om vår formel för ekvationen för den molekylär-kinetiska teorin för en idealgas i en tredje, annorlunda form:
p=1/3ρv^2.
Tja, det kanske är allt du behöver veta om det här ämnet. Det återstår bara att systematisera den kunskap som erhållits i form av korta (och inte så) slutsatser.
Alla allmänna slutsatser och formler om ämnet "Molekylär-kinetisk teori"
Så låt oss komma igång.
Först:
Fysik är en grundläggande vetenskap som ingår i naturvetenskapens kurs, som studerar materias och energis egenskaper, deras struktur, mönster av oorganisk natur.
Den innehåller följande avsnitt:
- mekanik (kinematik och dynamik);
- statisk;
- termodynamik;
- elektrodynamik;
- molekylär sektion;
- optik;
- kvanternas fysik och atomkärnan.
Andra:
Partikelfysik och termodynamik är närbesläktade grenar som studerar den uteslutande makroskopiska komponenten av det totala antalet fysiska system, det vill säga system som består av ett stort antal elementarpartiklar.
De är baserade på molekylär kinetisk teori.
Tredje:
Kärnpunkten i saken är detta. Den molekylära kinetiska teorin beskriver i detalj strukturen av ett ämne (oftare strukturen hos gaser än fasta ämnen).och flytande kroppar), baserat på tre grundläggande antaganden som samlades in från antaganden från framstående vetenskapsmän. Bland dem: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov och många andra.
Fjärde:
Tre grundläggande principer för molekylär kinetisk teori:
- Alla ämnen (oavsett om de är flytande, fasta eller gasformiga) har en komplex struktur som består av mindre partiklar: molekyler och atomer.
- Alla dessa enkla partiklar är i kontinuerlig kaotisk rörelse. Exempel: Brownsk rörelse och diffusion.
- Alla molekyler under alla förhållanden interagerar med varandra med vissa krafter som har en elektrisk sten.
Var och en av dessa bestämmelser i den molekylära kinetiska teorin är en solid grund i studiet av materiens struktur.
Femte:
Flera huvudpunkter i molekylär teori för gasmodellen:
- Alla gaser är uppbyggda av elementarpartiklar som inte har en viss storlek, men har en viss massa. Med andra ord är volymen av dessa partiklar minimal jämfört med avstånden mellan dem.
- Atomer och molekyler av gaser har praktiskt taget ingen potentiell energi, respektive, deras totala energi är lika med den kinetiska.
- Vi har redan bekantat oss med den här positionen tidigare - Brownsk rörelse. Det vill säga gaspartiklar är alltid i kontinuerlig och slumpmässig rörelse.
- Absolut alla ömsesidiga kollisioner av atomer och molekyler av gaser, åtföljda av budskapet om hastighet och energi, är helt elastiska. Detta ärbetyder att det inte sker någon energiförlust eller skarpa hopp i deras kinetiska energi under en kollision.
- Under normala förhållanden och konstant temperatur är den genomsnittliga kinetiska energin för nästan alla gaser densamma.
Sixth:
Slutsatser från teorin om gaser:
- Absolut temperatur är ett mått på den genomsnittliga kinetiska energin för dess atomer och molekyler.
- När två olika gaser har samma temperatur, har deras molekyler samma genomsnittliga kinetiska energi.
- Den genomsnittliga kinetiska energin för gaspartiklar är direkt proportionell mot rotens medelkvadrathastighet: E=1/2mv^2.
- Även om gasmolekyler har en genomsnittlig kinetisk energi respektive en medelhastighet, rör sig enskilda partiklar med olika hastigheter: vissa snabba, vissa långsamma.
- Ju högre temperatur, desto högre hastighet har molekylerna.
- Hur många gånger vi ökar temperaturen på gasen (till exempel fördubblas), den genomsnittliga kinetiska energin för dess partiklar ökar också så många gånger (fördubblas).
- Förhållandet mellan trycket från en gas på väggarna i kärlet där den är belägen och intensiteten av molekylers inverkan på dessa väggar är direkt proportionell: ju fler stötar, desto högre tryck, och vice versa.
sjunde:
En idealisk gasmodell är en modell där följande villkor måste uppfyllas:
- Gasmolekyler kan och anses vara perfekt elastiska bollar.
- Dessa bollar kan interagera med varandra och med väggarna på allafartyg i endast ett fall - absolut elastisk kollision.
- De krafterna som beskriver den ömsesidiga drivkraften mellan atomer och molekyler i en gas saknas eller kan faktiskt försummas.
- Atomer och molekyler betraktas som materiella punkter, det vill säga deras volym kan också försummas.
åttonde:
Låt oss ge alla grundläggande ekvationer och visa formlerna i ämnet "Molekylär-kinetisk teori":
p=1/3m(0)nv^2 - grundekvationen för den ideala gasmodellen, härledd av den tyske fysikern Rudolf Clausius.
p=2/3nE - den grundläggande ekvationen för den molekylär-kinetiska teorin för en idealgas. Härleds från den genomsnittliga kinetiska energin för molekylerna.
р=1/3ρv^2 - samma ekvation, men betraktad genom densiteten och rotmedelkvadrathastigheten för idealgasmolekyler.
m(0)=M/N(a) - formeln för att hitta massan av en molekyl genom Avogadro-talet.
v^2=(v(1)+v(2)+v(3)+…)/N - formel för att hitta medelkvadrathastigheten för molekyler, där v(1), v(2), v (3) och så vidare - hastigheten för den första molekylen, den andra, den tredje och så vidare upp till den n:e molekylen.
n=N/V - formel för att hitta koncentrationen av molekyler, där N är antalet molekyler i en gasvolym till en given volym V.
E=mv^2/2=3/2kT - formler för att hitta den genomsnittliga kinetiska energin för molekyler, där v^2 är rotmedelkvadrathastigheten för molekyler, k är en konstant värde uppkallat efter österrikaren Ludwig Boltzmanns fysik, och T är gasens temperatur.
p=nkT - tryckformel i termer av koncentration, konstantBoltzmann och den absoluta temperaturen T. Av den följer en annan grundläggande formel, upptäckt av den ryske vetenskapsmannen Mendeleev och den franske fysikern-ingenjören Claiperon:
pV=m/MRT, där R=kN(a) är den universella konstanten för gaser.
Låt oss nu visa konstanter för olika iso-processer: isobarisk, isokorisk, isotermisk och adiabatisk.
pV/T=const - utförs när gasens massa och sammansättning är konstanta.
рV=konst - om temperaturen också är konstant.
V/T=konst - om gastrycket är konstant.
p/T=konst - om volymen är konstant.
Det kanske är allt du behöver veta om det här ämnet.
Idag kastade vi oss in i ett sådant vetenskapligt område som teoretisk fysik, dess många sektioner och block. Mer detaljerat berörde vi ett sådant område av fysiken som fundamental molekylär fysik och termodynamik, nämligen molekylär-kinetisk teori, som, det verkar, inte har några svårigheter i den inledande studien, men i själva verket har många fallgropar. Det utökar vår förståelse av den ideala gasmodellen, som vi också studerade i detalj. Dessutom är det värt att notera att vi också har bekantat oss med de grundläggande ekvationerna för molekylär teori i deras olika variationer, och även övervägt alla de mest nödvändiga formlerna för att hitta vissa okända kvantiteter om detta ämne. Detta kommer att vara särskilt användbart när du förbereder dig för att skriva några tester, undersökningar och tester, eller för att utöka den allmänna synen och kunskaperna om fysik.
Vi hoppas att den här artikeln var användbar för dig, och du har bara extraherat den mest nödvändiga informationen från den, vilket stärker dina kunskaper om sådana pelare inom termodynamiken som de grundläggande bestämmelserna för molekylär kinetisk teori.






