I vår tid har fysik blivit en mycket vanlig vetenskap. Det finns bokstavligen överallt. Det mest elementära exemplet: ett äppelträd växer på din trädgård och frukter mognar på det, tiden kommer och äpplena börjar falla, men i vilken riktning faller de? Tack vare lagen om universell gravitation faller vårt foster till marken, det vill säga det går ner, men inte upp. Det var ett av de mest kända exemplen på fysik, men låt oss uppmärksamma termodynamiken, eller mer exakt, fasjämvikter, som inte är mindre viktiga i vårt liv.
Thermodynamics

Först av allt, låt oss titta på den här termen. ΘερΜοδυναΜική - så här ser ordet ut på grekiska. Den första delen ΘερΜo betyder "värme", och den andra δυναΜική betyder "styrka". Termodynamik är en gren av fysiken som studerar egenskaperna hos ett makroskopiskt system, samt olika sätt att omvandla och överföra energi. I detta avsnitt studeras olika tillstånd och processer speciellt för att begreppet temperatur ska kunna införas i beskrivningen (detta är en fysikalisk storhet som kännetecknar ett termodynamiskt system och mäts med hjälp avvissa apparater). Alla pågående processer i termodynamiska system beskrivs endast av mikroskopiska storheter (tryck och temperatur, samt koncentrationen av komponenter).
Clapeyron-Clausius ekvation
Varje fysiker känner till den här ekvationen, men låt oss bryta ner den bit för bit. Det hänvisar till jämviktsprocesserna för övergången av viss materia från en fas till en annan. Detta syns tydligt i sådana exempel: smältning, avdunstning, sublimering (ett av sätten att konservera produkter, vilket sker genom att helt avlägsna fukt). Formeln visar tydligt de pågående processerna:
- n=PV/RT;
- där T är ämnets temperatur;
- P-tryck;
- R-specifikt fasövergångsvärme;
- V-ändring i specifik volym.
Historien för skapandet av ekvationen

Clausius-Clapeyrons ekvation är en utmärkt matematisk förklaring av termodynamikens andra lag. Kallas även för "Clausius-ojämlikheten". Naturligtvis utvecklades satsen av vetenskapsmannen själv, som ville förklara sambandet mellan värmeflödet i systemet och entropin, såväl som dess miljö. Denna ekvation utvecklades av Clausius i hans försök att förklara och kvantifiera entropi. I bokstavlig mening ger satsen oss möjlighet att avgöra om en cyklisk process är reversibel eller irreversibel. Denna ojämlikhet erbjuder oss en kvantitativ formel för att förstå den andra lagen.
Forskaren var en av de första som arbetade med idén om entropi och gav den till och medprocess namn. Det som nu är känt som Clausius' teorem publicerades första gången 1862 i Rudolfs sjätte verk, On the Use of the Transformation Equivalence Theorem for Interior Work. Forskaren försökte visa ett proportionellt samband mellan entropi och energiflöde genom uppvärmning (δ Q) i systemet. I byggandet kan denna termiska energi omvandlas till arbete och den kan omvandlas till värme genom en cyklisk process. Rudolph bevisade att "den algebraiska summan av alla transformationer som sker i en cyklisk process bara kan vara mindre än noll eller, i extrema fall, lika med noll."
Stängt isolerat system
Isolerat system är ett av följande:
- Det fysiska systemet är långt ifrån andra som inte interagerar med dem.
- Det termodynamiska systemet är stängt av styva orörliga väggar genom vilka varken materia eller energi kan passera.
Trots att ämnet är internt relaterat till sin egen gravitation, tas ett isolerat system vanligtvis bortom gränserna för yttre gravitationskrafter och andra avlägsna krafter.
Detta kan jämföras med det som (i den mer allmänna terminologin som används inom termodynamiken) kallas ett slutet system omgivet av selektiva väggar genom vilka energi kan överföras i form av värme eller arbete, men inte materia. Och med ett öppet system där materia och energi kommer in eller ut, även om det kan ha olika ogenomträngliga väggar idelar av dess gränser.
Ett isolerat system följer naturvårdslagen. Oftast inom termodynamiken betraktas materia och energi som separata begrepp.
Termodynamiska övergångar
För att förstå kvantfasövergångar är det användbart att jämföra dem med klassiska transformationer (även kallade termiska inversioner). CPT beskriver spetsen i de termodynamiska egenskaperna hos ett system. Det signalerar omorganisationen av partiklar. Ett typiskt exempel är den frysande övergången av vatten, som beskriver en mjuk övergång mellan en vätska och en fast substans. Klassisk fastillväxt beror på konkurrensen mellan systemets energi och entropin i dess termiska fluktuationer.
Ett klassiskt system har ingen entropi vid nolltemperatur och därför kan ingen fastransformation inträffa. Deras ordning bestäms av den första diskontinuerliga termodynamiska derivatans potential. Och naturligtvis har den första ordningen. Fasomvandlingar från en ferromagnet till en paramagnet är kontinuerliga och andra ordningens. Dessa konstanta förändringar från en ordnad till en oordnad fas beskrivs av en ordningsparameter som är noll. För ovanstående ferromagnetiska transformation kommer orderparametern att vara den totala magnetiseringen av systemet.
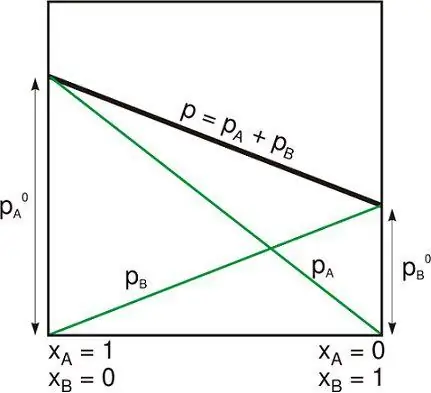
Gibbs potential
Gibbs Free Energy är den maximala mängden arbete utan expansion som kan tas bort från ett termodynamiskt slutet system (som kan utbyta värme och arbeta med miljön). Sådandet maximala resultatet kan endast erhållas i en helt reversibel process. När systemet transformerar tillbaka från det första tillståndet till det andra är minskningen av Gibbs fria energi lika med den som utförs av systemet i dess omgivning, minus tryckkrafternas arbete.
Saldotillstånd

Termodynamisk och mekanisk jämvikt är ett axiomatiskt begrepp inom termodynamiken. Detta är det interna tillståndet för ett eller flera system som är förbundna med mer eller mindre permeabla eller ogenomträngliga väggar. I detta tillstånd finns det inga rena makroskopiska flöden av materia eller energi, varken inom ett system eller mellan system.
I sin egen uppfattning om tillståndet för inre jämvikt sker ingen makroskopisk förändring. Systemen befinner sig samtidigt i ömsesidig termisk, mekanisk, kemisk (konstant), strålningsjämvikt. De kan vara i samma form. I denna process sparas alla vyer på en gång och på obestämd tid tills den fysiska operationen avbryts. I makroskopisk jämvikt sker perfekt exakta balanserade utbyten. Ovanstående bevis är en fysisk förklaring av detta koncept.
Basics
Varje lag, satser, formler har sin egen grund. Låt oss titta på de tre grunderna för lagen om fasjämvikt.
- Fas är en form av materia, homogen i kemisk sammansättning, fysikaliskt tillstånd och mekanisk balans. Typiska faser är fasta, flytande och gasformiga. Två oblandbara vätskor (eller flytande blandningar med olika sammansättning) åtskilda av en separat gräns anses vara två distinkta faser och oblandbara fasta ämnen.
- Antalet komponenter (C) är antalet kemiskt oberoende komponenter i systemet. Det minsta antal oberoende arter som krävs för att bestämma sammansättningen av alla faser i systemet.
- Antalet frihetsgrader (F) i detta sammanhang är antalet intensiva variabler som är oberoende av varandra.
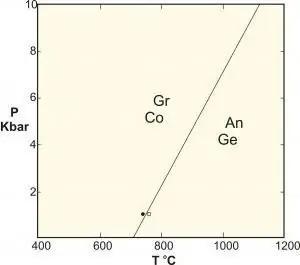
Klassificering efter fasjämvikt
- Reaktioner av kontinuerlig nettoöverföring (ofta kallade solid state-reaktioner) inträffar mellan fasta ämnen med olika sammansättning. De kan inkludera element som finns i vätskor (H, C), men dessa element hålls kvar i fasta faser, så inga flytande faser är inblandade som reaktanter eller produkter (H2O, CO2). Fasta rena överföringsreaktioner kan vara kontinuerliga eller diskontinuerliga, eller terminala.
- Polymorfa är en speciell typ av fastfasreaktion som inkluderar faser med identisk sammansättning. Klassiska exempel är reaktionerna mellan aluminiumsilikater kyanit-sillimanit-andalusit, omvandlingen av grafit till diamant vid högt tryck och jämvikten av kalciumkarbonat.
Jämviktslagar

The Gibbs Factory Rule föreslogs av Josiah Willard Gibbs i hans berömda artikel med titeln "The Equilibrium of Heterogeneous Substances", som kom från 1875 till 1878. Det gällericke-reaktiva multikomponent heterogena system i termodynamisk jämvikt och är en given likhet:
- F=C-P+2;
- där F är antalet frihetsgrader;
- C - antal komponenter;
- P - antal faser i termodynamisk jämvikt med varandra.
Antalet frihetsgrader är antalet obesatta intensivvariabler. Det största antalet termodynamiska parametrar, såsom temperatur eller tryck, som kan variera samtidigt och godtyckligt utan att påverka varandra. Ett exempel på ett enkomponentsystem är ett med en enda ren kemikalie, medan tvåkomponentsystem, såsom blandningar av vatten och etanol, har två oberoende komponenter. Typiska fasövergångar (fasjämvikt) är fasta ämnen, vätskor, gaser.
Fasregel vid konstant tryck
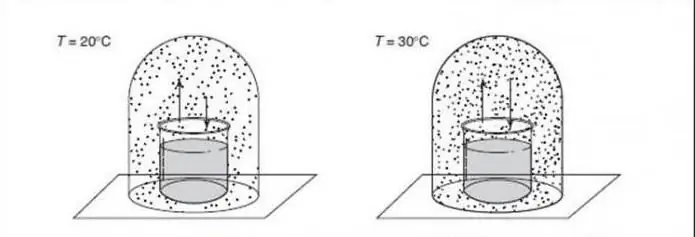
För tillämpningar inom materialvetenskap som handlar om fasförändringar mellan olika fasta strukturer uppstår ofta ett konstant tryck (t.ex. en atmosfär) och ignoreras som en frihetsgrad, så regeln blir: F=C - P + 1.
Denna formel introduceras ibland under namnet "regel för kondenserad fas", men som vi vet är den inte tillämpbar på dessa system som utsätts för höga tryck (till exempel inom geologi), eftersom konsekvenserna av dessa tryck kan orsaka katastrofala konsekvenser.
Det kan verka som att fasjämvikt bara är en tom fras, och det finns få fysiska processer där detta ögonblickär inblandad, men, som vi har sett, utan det fungerar många av de lagar vi känner inte, så du måste bekanta dig lite med dessa unika, färgglada, om än lite tråkiga regler. Denna kunskap har hjälpt många människor. De lärde sig att tillämpa dem på sig själva, till exempel kan elektriker, som känner till reglerna för att arbeta med faser, skydda sig mot onödiga faror.

