Molekylär-kinetisk teori gör det möjligt att, genom att analysera systemets mikroskopiska beteende och använda metoderna för statistisk mekanik, erhålla viktiga makroskopiska egenskaper hos det termodynamiska systemet. En av de mikroskopiska egenskaperna, som är relaterad till systemets temperatur, är medelkvadrathastigheten för gasmolekyler. Vi ger formeln för det och överväger det i artikeln.
Ideal gas
Vi noterar direkt att formeln för den kvadratiska medelhastigheten för gasmolekyler kommer att ges specifikt för en ideal gas. Under det, i fysiken, betraktas ett sådant många-partikelsystem där partiklar (atomer, molekyler) inte interagerar med varandra (deras kinetiska energi överstiger den potentiella energin för interaktion med flera storleksordningar) och inte har dimensioner, det vill säga de är punkter med en ändlig massa (avståndet mellan partiklar som är flera storleksordningar större än deras storlek.linjär).
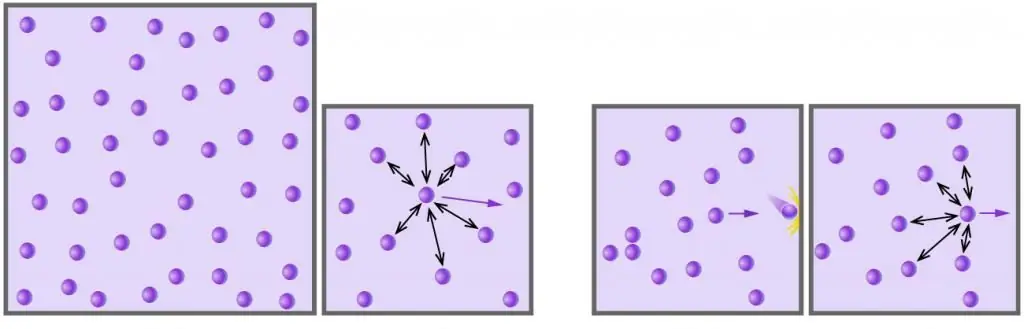
Varje gas som helst som består av kemiskt neutrala molekyler eller atomer, och som står under lågt tryck och har en hög temperatur, kan anses vara idealisk. Luft är till exempel en idealisk gas, men vattenånga är inte längre sådan (starka vätebindningar verkar mellan vattenmolekyler).
Molecular Kinetic Theory (MKT)

När du studerar en idealisk gas inom ramen för MKT bör du vara uppmärksam på två viktiga processer:
- Gas skapar tryck genom att överföra momentumet när molekyler och atomer kolliderar med dem till väggarna i kärlet som innehåller den. Sådana kollisioner är helt elastiska.
- Molekyler och gasatomer rör sig slumpmässigt i alla riktningar med olika hastigheter, vars fördelning följer Maxwell-Boltzmanns statistik. Sannolikheten för kollision mellan partiklar är extremt låg, på grund av deras försumbara storlek och stora avstånd mellan dem.
Trots att de individuella hastigheterna för gaspartiklar skiljer sig mycket från varandra, förblir medelvärdet av detta värde konstant över tiden om det inte finns någon yttre påverkan på systemet. Formeln för medelkvadrathastigheten för gasmolekyler kan erhållas genom att beakta sambandet mellan kinetisk energi och temperatur. Vi kommer att ta itu med det här problemet i nästa stycke i artikeln.
Herledning av formeln för den kvadratiska medelhastigheten för idealgasmolekyler
Varje elev vet från den allmänna fysikkursen att den kinetiska energin för translationsrörelsen hos en kropp med massan m beräknas enligt följande:
Ek=mv2/2
Där v är den linjära hastigheten. Å andra sidan kan den kinetiska energin för en partikel också bestämmas i termer av den absoluta temperaturen T, med hjälp av omvandlingsfaktorn kB(Boltzmanns konstant). Eftersom vårt utrymme är tredimensionellt beräknas Ek enligt följande:
Ek=3/2kBT.
Motsvarar båda likheterna och uttrycker v från dem, erhåller vi formeln för medelhastigheten för en kvadratisk idealgas:
mv2/2=3/2kBT=>
v=√(3kBT/m).
I denna formel är m - gaspartikelns massa. Dess värde är obekvämt att använda i praktiska beräkningar, eftersom det är litet (≈ 10-27kg). För att undvika detta besvär, låt oss komma ihåg den universella gaskonstanten R och den molära massan M. Konstanten R med kB är relaterad till likheten:
kB=R/NA.
Värdet på M definieras enligt följande:
M=mNA.
Med hänsyn till båda likheterna får vi följande uttryck för rot-medelkvadrathastigheten för molekyler:
v=√(3RT/M).
Således är medelkvadrathastigheten för gaspartiklar direkt proportionell mot kvadratroten ur absolut temperatur och omvänt proportionell mot kvadratroten av molmassan.
Exempel på problemlösning
Alla vet att luften vi andas är 99 % kväve och syre. Det är nödvändigt att bestämma skillnaderna i medelhastigheterna för molekylerna N2 och O2 vid en temperatur av 15 o C.

Detta problem kommer att lösas sekventiellt. Först översätter vi temperaturen till absoluta enheter, vi har:
T=273, 15 + 15=288, 15 K.
Skriv nu ut molmassorna för varje molekyl som övervägs:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Eftersom värdena på molära massor skiljer sig något, bör deras medelhastigheter vid samma temperatur också vara nära. Med formeln för v får vi följande värden för kväve- och syremolekyler:
v (N2)=√(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473,9 m/s.
Eftersom kvävemolekyler är något lättare än syremolekyler, rör de sig snabbare. Den genomsnittliga hastighetsskillnaden är:
v (N2) - v (O2)=506,6 - 473,9=32,7 m/s.
Det resulterande värdet är bara 6,5 % av medelhastigheten för kvävemolekyler. Vi uppmärksammar molekylernas höga hastigheter i gaser, även vid låga temperaturer.






